Bảng nguyên tử khối của các chất thường gặp gồm đầy đủ thông tin của các chất trong chương trình hóa học lớp 8 và hóa học lớp 9. Để làm được bài tập tính toán, các em cần phải nắm vững được nguyên tử khối của các chất. Do vậy bảng nguyên tử khối sẽ là tài liệu vô cùng quan trọng.
Định nghĩa nguyên tử khối
Giới thiệu
Ngay từ khi bắt đầu với môn hóa học, các em đã có trong đầu những khái niệm cơ bản như là số proton, công thức hóa học, kí hiệu hóa học, nguyên tử khối của một chất hay cụ thể hơn trong hóa học thường nhắc tới hóa trị.
Để giúp các em cần nhớ những thông tin bên trên của những nguyên tố rất thường gặp trong chương trình hóa học lớp 8, chương trình hóa học lớp 9. HoaHoc24h đã có thống kê lại ở bảng bên dưới được gọi chung là bảng nguyên tử khối của các chất thường gặp trong chương trình hóa học.
Nguyên tử khối là gì?
Nguyên tử khối của một nguyên tử là khối lượng của một nguyên tử tính bằng đơn vị Cacbon. Hiểu rộng ra, nguyên tử khối chính là khối lượng của một nguyên tử mà trong đó là tổng khối lượng của các hạt cấu tạo nên nguyên tử. Các hạt cấu tạo nên nguyên tử gồm: Hạt proton, electron và notron.
Bằng thực nghiệm, nhà khoa học đã chúng minh được khối lượng của electron tương đối nhỏ nên chúng ta thường không tính và cũng chính vì thế mà nguyên tử khối được tính xấp xỉ bằng số khối của hạt nhân.
Nguyên tử khối có quan trọng không?
Nguyên tử khối của một chất là rất quan trọng với mỗi học sinh. Khi biết được nguyên tử khối của một chất chúng ta có thể biết được chất đó là chất nào. Nguyên tử khối rất quan trọng trong những bài toán lập công thức hóa học của hợp chất hoặc những bài tập liên quan tới tính toán hóa học.
Khi nắm được nguyên tử khối của càng nhiều chất thì các em sẽ càng giải những bài toán hóa học đơn giản hơn. Nguyên tử khối có thể coi là cánh cửa đi vào hóa học. Cũng chính vì lý do trên, nhóm Hóa Học 24H đã lập một bảng nguyên tử khối giúp các em yên tâm phần nào khi tìm hiểu kiến thức trên mạng.
Nếu như các em học thuộc được nguyên tử khối của những chất có trong bảng bên dưới thì thầy chắc chắn các em sẽ học tốt môn hóa học sau này.
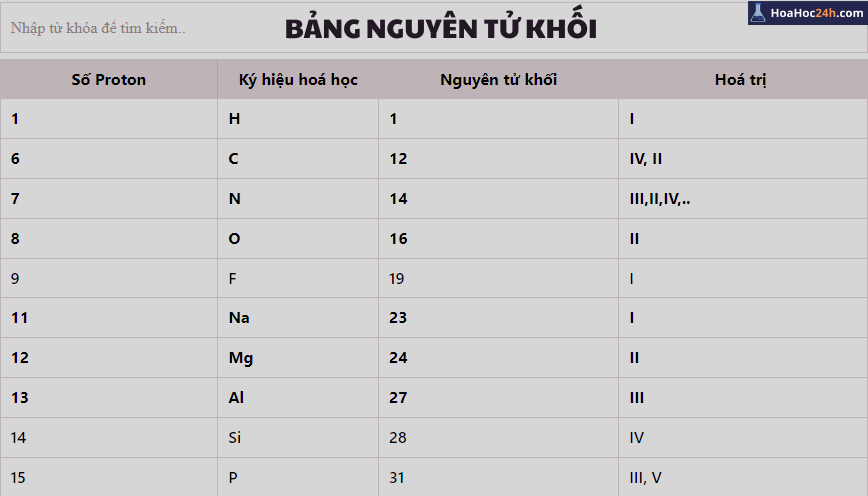
Bảng nguyên tử khối của các chất thường gặp
| Số Proton | Ký hiệu hoá học | Nguyên tử khối | Hoá trị |
|---|---|---|---|
| 1 | H | 1 | I |
| 6 | C | 12 | IV, II |
| 7 | N | 14 | III,II,IV,.. |
| 8 | O | 16 | II |
| 9 | F | 19 | I |
| 11 | Na | 23 | I |
| 12 | Mg | 24 | II |
| 13 | Al | 27 | III |
| 14 | Si | 28 | IV |
| 15 | P | 31 | III, V |
| 16 | S | 32 | II,IV,VI,.. |
| 17 | Cl | 35,5 | I,.. |
| 19 | K | 39 | I |
| 20 | Ca | 40 | II |
| 26 | Fe | 56 | II,III |
| 29 | Cu | 64 | I,II |
| 30 | Zn | 65 | II |
| 35 | Br | 80 | I,… |
| 47 | Ag | 108 | I |
| 56 | Ba | 137 | II |
| 80 | Hg | 201 | I,II |
| 82 | Pb | 207 | II,IV |
Nguyên tử khối của một số nguyên tố thường gặp
Hidro (H)
– Nguyên tố Hidro kí hiệu hóa học là H nguyên tử khối của nguyên tố Hidro là 1. Hợp chất có chứa nguyên tố hidro thường gặp là H2O, HCl, H2SO4, H2S, HNO3 . . . chủ yếu gặp trong các chất là axit. Sau này, nguyên tố hidro thường xuất hiện trong hợp chất hữu cơ.
– Nguyên tố Cacbon đọc là Các bon kí hiệu hóa học là C nguyên tử khối của cacbon là 12. Hợp chất có chứa nguyên tố cacbon thường gặp CO2, H2CO3, CaCO3 . . .
– Nguyên tố Oxi có kí hiệu hóa học là O nguyên tử khối của oxi là 16. Hợp chất có chứa nguyên tố oxi thường gặp là những hợp chất ở bên trên và cho chúng ta thấy nguyên tố oxi hầu hết có mặt trong các hợp chất nên các em cần thuộc lòng về nguyên tố oxi.
Oxi (O)
– Kí hiệu hóa học: O
– Hóa trị của oxi: II
– Số proton: 08
– Số electron: 08
– Nguyên tử khối: 16
– Cấu hình electron của oxi: [He] 2s²2p⁴
Cách tính phân tử khối của hợp chất hóa học
Để tính phân tử khối hay còn được gọi là cách tính khối lượng mol của hợp chất hóa học, chúng ta cần phải biết được chất đó được cấu tạo nên bởi nguyên tố nào. Từ nguyên tố cấu tạo chúng ta biết được nguyên tử khối của nguyên tố đó là bao nhiêu và phân tử khối của hợp chất hóa học đó được tính bằng cách lấy tổng nguyên tử khối của các nguyên tố cấu tạo nên nhân với chỉ số đi kèm trong công thức hóa học.
Cách tính phân tử khối tổng quát
Xét một chất tổng quát có công thức hóa học là AaBb
Trong đó:
– A, B là nguyên tố hóa học cấu tạo nên hợp chất trên.
– a, b là số lượng nguyên tử của mỗi nguyên tố tương ứng.
Phân tử khối của hợp chất trên được tính như sau:
Phân tử khối = [Nguyên tử khối của]A x a + [Nguyên tử khối của]B x b
– x là dấu nhân.
Bài toán tính phân tử khối của các hợp chất hóa học
Tính phân tử khối của hợp chất hóa học:
– Đồng (II) Oxit có công thức hóa học là CuO
– Nhôm (III) Oxit có công thức hóa học là Al2O3
– Natri Sunfat có công thức hóa học là Na2SO4
– Sắt (II) Oxit có công thức hóa học là FeO
– Sắt (III) Oxit có công thức hóa học là Fe2O3
– Sắt từ Oxit có công thức hóa học là Fe3O4
Ở ví dụ này, các em áp dụng cách tính phân tử khối như trên là sẽ tính được thôi. Chỉ có điều, các em cần biết được nguyên tử khối của các nguyên tố cấu tạo nên phân tử đó.

Với đam mê truyền đạt và chia sẻ những kiến thức hóa học hữu ích với mọi người, TC Chemistry không chỉ giới hạn việc chia sẻ kiến thức hóa học từ cơ bản đến nâng cao, mà còn cung cấp câu hỏi, đề thi thử và phương trình phản ứng hóa học để giúp người đọc hiểu sâu về chủ đề và phát triển kỹ năng trong lĩnh vực này.