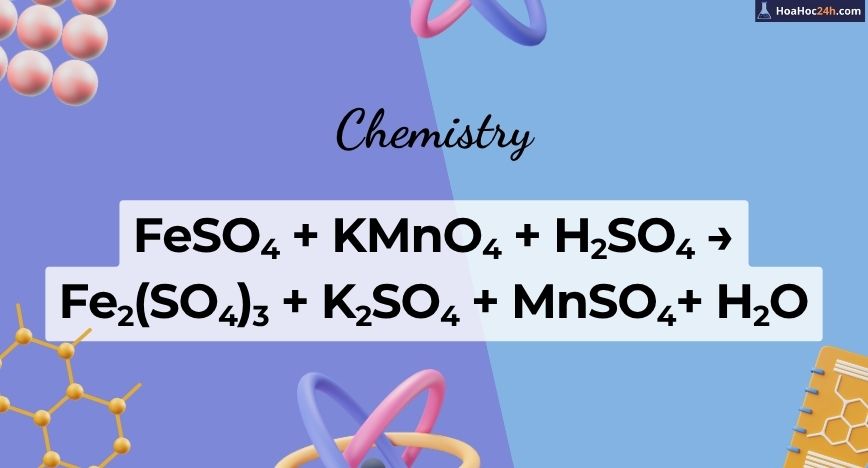
Phản ứng giữa muối sắt(II) sunfat (FeSO₄) và kali pemanganat (KMnO₄) trong môi trường axit sunfuric (H₂SO₄) là một phản ứng oxi hóa – khử, trong đó ion Fe²⁺ bị oxi hóa thành Fe³⁺ và ion MnO₄⁻ bị khử thành Mn²⁺. Quá trình diễn ra trong môi trường axit mạnh, đòi hỏi sự có mặt […]
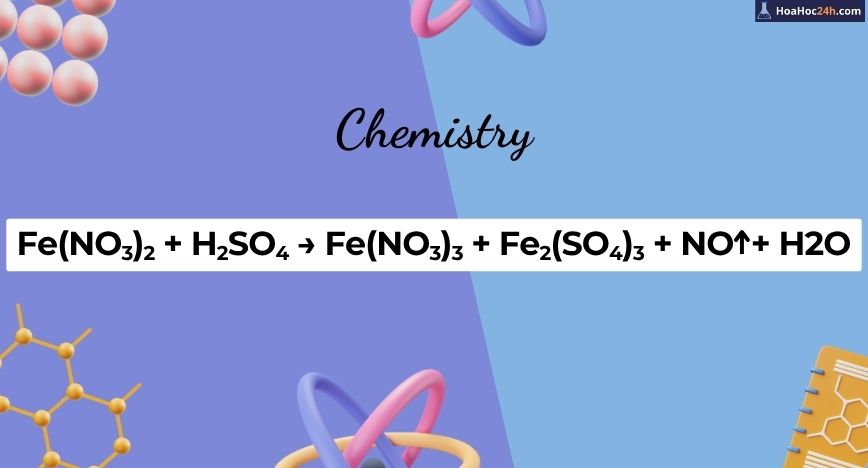
Fe(NO3)2 + H2SO4 → Fe2(SO4)3 + Fe(NO3)3 + NO +H2O
Phản ứng giữa Fe(NO₃)₂ và H₂SO₄ là một ví dụ tiêu biểu cho hiện tượng nội phân tử oxi hóa – khử, nơi Fe²⁺ bị oxi hóa, còn NO₃⁻ đồng thời bị khử trong cùng một hệ, dưới tác dụng của axit mạnh H₂SO₄. Đây là một cơ chế phổ biến trong hóa học vô […]
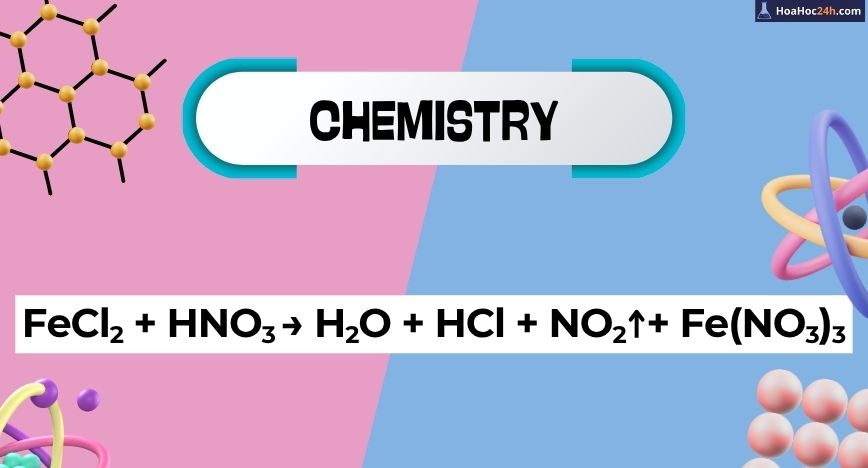
FeCl2 + HNO3 → H2O + HCl + NO2 + Fe(NO3)3
Phản ứng giữa sắt(II) clorua (FeCl₂) và axit nitric (HNO₃) là một ví dụ điển hình trong hóa học vô cơ về sự kết hợp giữa cơ chế oxi hóa – khử và sự thay thế anion trong muối. Tính phức tạp của phản ứng này đến từ việc HNO₃ không chỉ là một axit […]
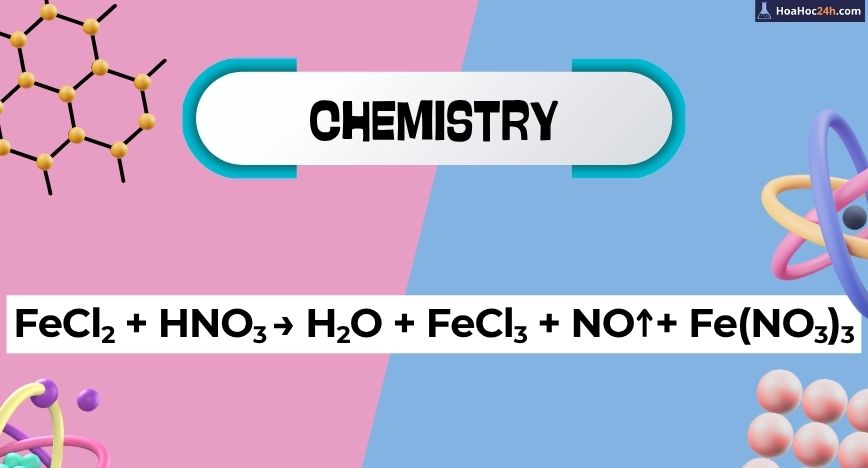
FeCl2 + HNO3 → H2O + NO + Fe(NO3)3 + FeCl3
Phản ứng giữa sắt(II) clorua (FeCl₂) và axit nitric (HNO₃) là một ví dụ điển hình trong hóa học vô cơ về sự kết hợp giữa cơ chế oxi hóa – khử và sự thay thế anion trong muối. Tính phức tạp của phản ứng này đến từ việc HNO₃ không chỉ là một axit […]
FeCl2 + Cl2 → FeCl3
Phản ứng giữa Sắt(II) Clorua (FeCl₂) và khí Clo (Cl₂) là một phản ứng oxi hóa – khử, trong đó Fe²⁺ trong FeCl₂ bị oxi hóa thành Fe³⁺, tạo Sắt(III) Clorua (FeCl₃). Cl₂ đóng vai trò chất oxi hóa, bị khử thành Cl⁻. Phản ứng này là một phản ứng xảy ra giữa một ion […]