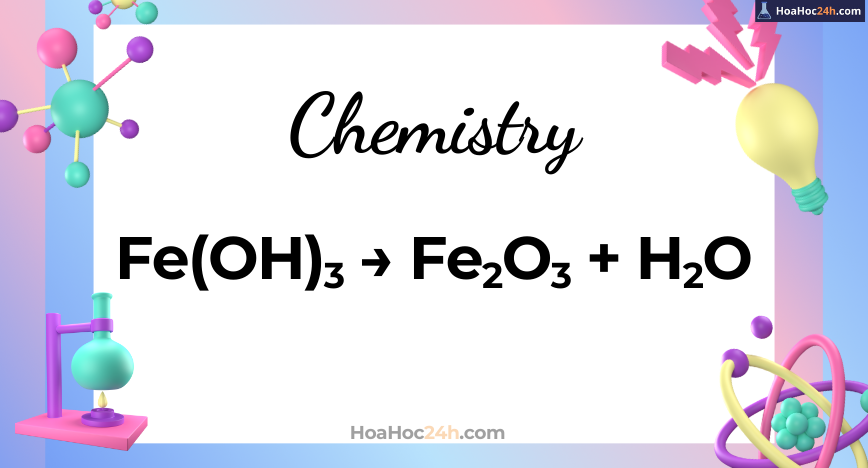
Phản ứng phân hủy sắt(III) hiđroxit (Fe(OH)₃) tạo thành sắt(III) oxit (Fe₂O₃) và nước là một ví dụ điển hình của phản ứng nhiệt phân trong hóa vô cơ. Phản ứng này thường được khảo sát trong chương trình trung học phổ thông và có ý nghĩa trong việc minh họa sự thay đổi trạng […]
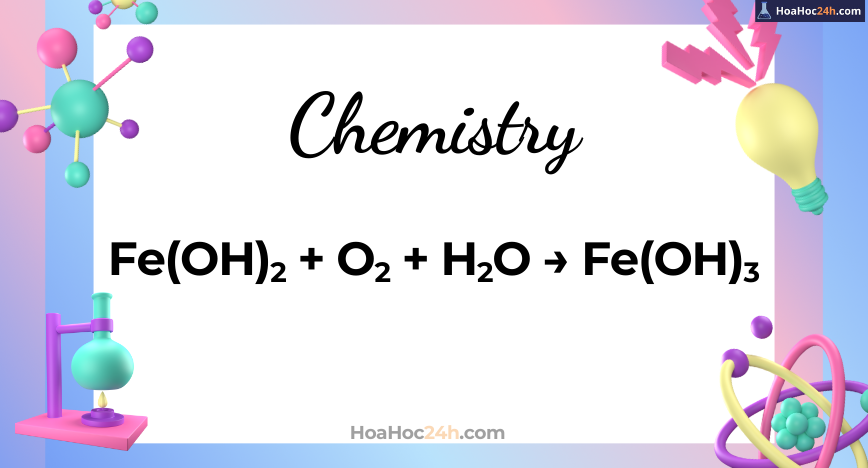
Fe(OH)2 + O2 + H2O → Fe(OH)3
Phản ứng giữa hiđroxit sắt(II) Fe(OH)₂ với oxy và nước tạo thành hiđroxit sắt(III) Fe(OH)₃ là quá trình oxy hóa trong môi trường nước. Đây là một ví dụ điển hình cho phản ứng oxy hóa – khử trong dung dịch, đồng thời cũng phản ánh bản chất chuyển hóa hóa trị của kim loại […]
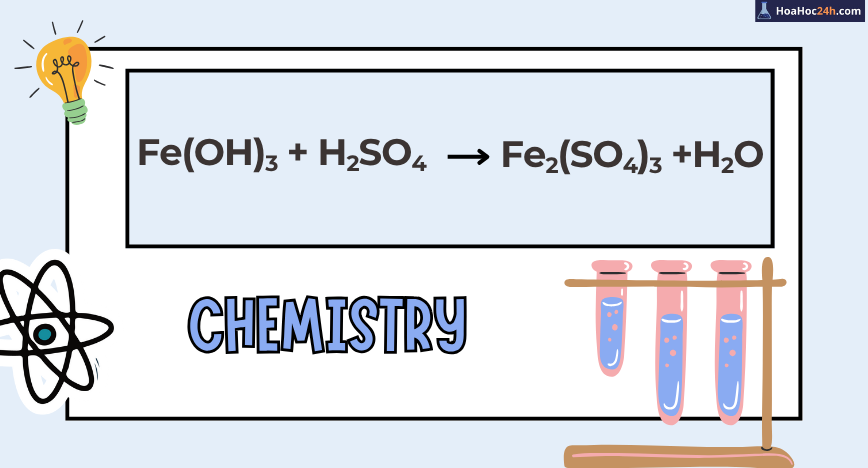
Fe(OH)3 + H2SO4 → Fe2(SO4)3 + H2O
Phản ứng giữa Sắt (III) Hydroxide (Fe(OH)₃) và Axit Sulfuric (H₂SO₄) là một phản ứng trung hòa axit – bazơ đặc trưng, thể hiện tính chất của oxit bazơ. Fe(OH)₃ tác dụng với H₂SO₄ tạo ra muối Sắt(III) Sulfat (Fe₂(SO₄)₃) và nước (H₂O). Phản ứng giúp ta hiểu cách oxit kim loại phản ứng với axit […]
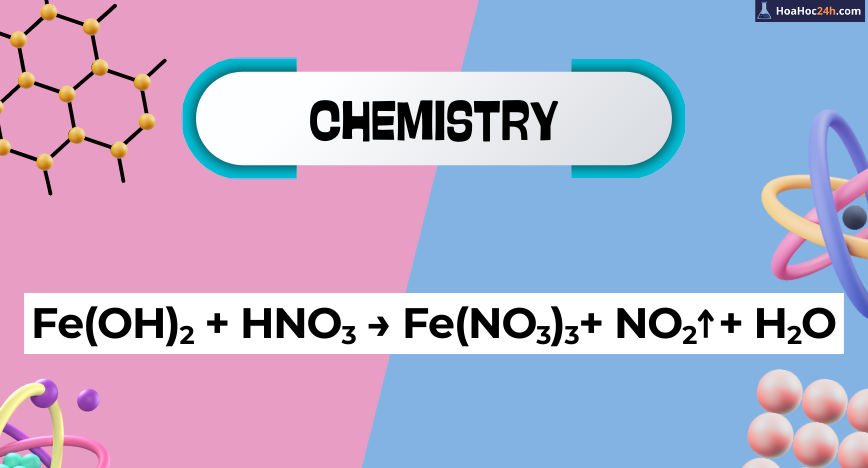
Fe(OH)2 + HNO3 → Fe(NO3)3 + NO2 + H2O
Phản ứng giữa Sắt(II) Hidroxit (Fe(OH)₂) và Axit Nitric (HNO₃) là một phản ứng oxi hóa – khử đặc trưng. Trong điều kiện sử dụng HNO₃ đậm đặc và gia nhiệt mạnh, trong đó Fe(OH)₂ bị oxi hóa tạo ra sắt(III) nitrat (Fe(NO₃)₃), nước (H₂O), và khí nitơ dioxit (NO₂↑). Phản ứng này minh họa […]
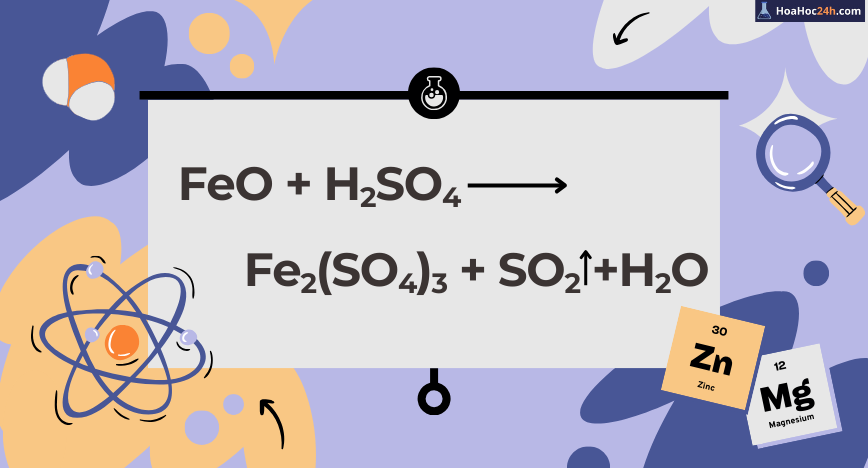
FeO + H2SO4 → Fe2(SO4)3 + H2O + SO2
Khi axit sunfuric đậm đặc, nóng tác dụng với oxit kim loại như FeO, phản ứng không còn là trung hòa đơn thuần nữa mà là phản ứng oxi hóa – khử phức tạp. Trong phản ứng này, FeO không chỉ phản ứng như một oxit bazơ mà còn bị oxi hóa từ Fe²⁺ → […]