Bảng hóa trị của một số nguyên tố hóa học thường được sử dụng trong chương trình hóa học lớp 8 là tài liệu vô cùng bổ ích giúp các em nằm được những thông tin mà mình cần phải trang bị trước khi bước vào những kỳ thi căng thẳng.
Hóa trị là gì?
Hóa trị của một nguyên tố hóa học được xác định bằng tổng số liên kết hóa học của nguyên tố đó tạo nên trong phân tử. Với hóa trị của một nguyên tố thì thầy cũng đã có một bài viết khác chia sẻ với các em nhiều hơn về hóa trị của một nguyên tố.
Trong bài viết này, thầy chỉ chia sẻ hóa trị của một số nguyên tố thường gặp trong chương trình hóa học lớp 8 giúp các em có thêm tư liệu, tài liệu để củng cố kiến thức hóa học cơ bản của mình nhé. Các em có thể tham khảo thêm bảng hóa trị lớp 8 trang 42 trong SGK nhé.
Bảng hóa trị nguyên tố hóa học thường gặp
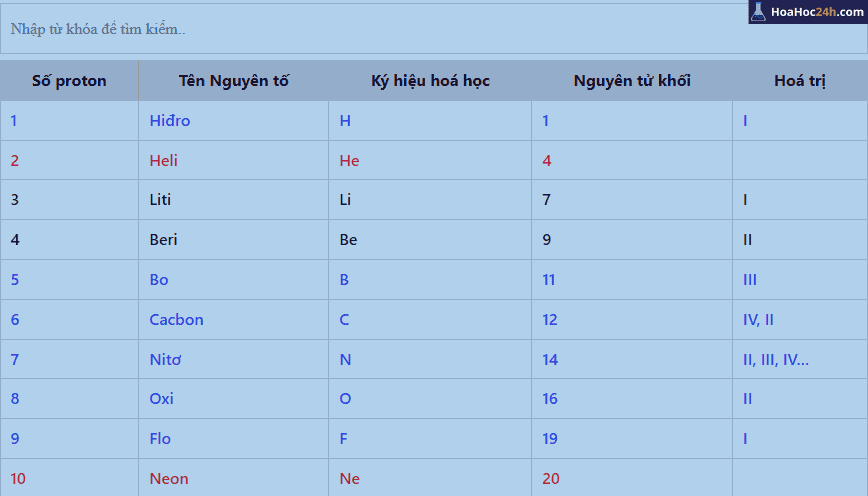
Bảng hóa trị bao gồm có một số thông tin như Số Proton, tên nguyên tố, ký hiệu hóa học, nguyên tử khối và cột cuối cùng có thể hiện hóa trị của nguyên tố đó theo chữ cái la mã. Bảng hóa trị dưới đây bao gồm tất cả có 30 nguyên tố hóa học thường xuất hiện trong chương trình học hóa học lớp 8.
Một số lưu ý với những nguyên tố có nhiều hóa trị thường gặp như kim loại có sắt, đồng . . . còn đa phần nhiều nguyên tố phi kim sẽ có nhiều mức hóa trị khác nhau như Nito, lưu huỳnh, phốt pho …
| Số proton | Tên Nguyên tố | Ký hiệu hoá học | Nguyên tử khối | Hoá trị |
|---|---|---|---|---|
| 1 | Hiđro | H | 1 | I |
| 2 | Heli | He | 4 | |
| 3 | Liti | Li | 7 | I |
| 4 | Beri | Be | 9 | II |
| 5 | Bo | B | 11 | III |
| 6 | Cacbon | C | 12 | IV, II |
| 7 | Nitơ | N | 14 | II, III, IV… |
| 8 | Oxi | O | 16 | II |
| 9 | Flo | F | 19 | I |
| 10 | Neon | Ne | 20 | |
| 11 | Natri | Na | 23 | I |
| 12 | Magie | Mg | 24 | II |
| 13 | Nhôm | Al | 27 | III |
| 14 | Silic | Si | 28 | IV |
| 15 | Photpho | P | 31 | III, V |
| 16 | Lưu huỳnh | S | 32 | II, IV, VI |
| 17 | Clo | Cl | 35,5 | I,… |
| 18 | Argon | Ar | 39,9 | |
| 19 | Kali | K | 39 | I |
| 20 | Canxi | Ca | 40 | II |
| 24 | Crom | Cr | 52 | II, III |
| 25 | Mangan | Mn | 55 | II, IV, VII… |
| 26 | Sắt | Fe | 56 | II, III |
| 29 | Đồng | Cu | 64 | I, II |
| 30 | Kẽm | Zn | 65 | II |
| 35 | Brom | Br | 80 | I… |
| 47 | Bạc | Ag | 108 | I |
| 56 | Bari | Ba | 137 | II |
| 80 | Thuỷ ngân | Hg | 201 | I, II |
| 82 | Chì | Pb | 207 | II, IV |
Lưu ý
- Nguyên tố kim loại có chữ màu đen
- Nguyên tố phi kim có chữ màu xanh
- Nguyên tố khí hiếm có chữ màu đỏ
Bảng hóa trị của các gốc – nhóm chức
| STT | Tên gốc – nhóm chức | Công thức hóa học nhóm – gốc axit | Nguyên tử khối | Hóa Trị |
|---|---|---|---|---|
| 1 | Hidroxit | OH | 17 | I |
| 2 | Clorua | Cl | 35,5 | I |
| 3 | Nitrat | NO3 | 62 | I |
| 4 | Sunfat | SO4 | 96 | II |
| 5 | Cacbonat | CO3 | 60 | II |
| 6 | Clorat | ClO3 | 83.5 | I |
| 7 | Perclorat | ClO4 | 99.5 | I |
| 8 | ĐiHidro Photphat | H2PO4 | 98 | I |
| 9 | Hidro Photphat | HPO4 | 97 | II |
| 10 | Photphat | PO4 | 96 | III |
Bảng hóa trị ở trên là bảng hóa trị của các gốc – nhóm chức có thể liên kết với nguyên tố hóa học hay nhóm nguyên tố hóa học khác tạo thành các hợp chất hóa học khác nhau.
Ví dụ Natri liên kết với gốc -Cl tạo thành muối NaCl.
Bảng hóa trị một số nhóm nguyên tử
| Tên nhóm | Hoá trị | Gốc axit | Axit tương ứng | Tính axit |
|---|---|---|---|---|
| Hiđroxit (*) (OH); Nitrat (NO3) | I | NO3 | HNO3 | Mạnh |
| Sunfat (SO4); Cacbonat (CO3) | II | SO4 | H2SO4 | Mạnh |
| Photphat (PO4) | I, II, III | Cl | HCl | Mạnh |
| (*): Tên này dùng trong các hợp chất với kim loại. | PO4 | H3PO4 | Trung bình | |
| CO3 | H2CO3 | Rất yếu (không tồn tại) | ||
Bảng hóa trị trên được các em biết đến trong chương trình hóa học lớp 8 gồm hóa trị của một số nhóm nguyên tử như:
– Hóa trị của nhóm -OH là I
– Hóa trị của nhóm -NO3 là I
– Hóa trị của nhóm =SO4 là II
– Hóa trị của nhóm =CO3 là II
Nhóm nguyên tố có nhiều hóa trị PO4
Một trong những nhóm nguyên tố có số hóa trị nhiều mà chúng ta thường gặp nhất đó chính là nhóm (PO4) bởi vì chúng ta sẽ gặp nhóm này có hóa trị I hoặc PO4 có hóa trị II hoặc PO4 có hóa trị là III cụ thể như sau:
PO4 là gốc axit của Axit phosphoric có công thức hóa học đầy đủ là H3PO4. Đây là một axit có tính oxi hóa trung bình nhưng chúng lại tẹo nên rắc rối cho học sinh bởi nó có thể tạo thành 2 loại muối với 3 công thức khác nhau.
Muối axit chứa gốc PO4
H3PO4 có thể tạo muối axit trong hai công thức M(H2PO4)x và M2(HPO4)x với M là kim loại nào đó. Nhìn vào công thức trên chúng ta sẽ thấy rắc rối lắm phải không, vậy thì hãy quan sát hợp chất cụ thể dưới đây nhé.
Lấy M là kim loại Natri có hóa trị 1 chúng ta được:
– Na(H2PO4)
– Na2(HPO4)
Trên đó chính là 2 công thức muối axit.
Muối trung hòa chứa gốc PO4
Công thức muối trung hòa có chứa gốc PO4 có dạng: M3(PO4)x với:
- M là kim loại
- x là số hóa trị của kim loại M.
Bảng hóa trị nguyên tố hóa trị I
Bảng hóa trị thông thường tập hợp hóa trị của nhiều nguyên tố khác nhau do vậy bảng hóa trị này sẽ giúp học sinh tổng hợp lại những nguyên tố có hóa trị I như vậy sẽ dễ nhớ hơn rất nhiều.
Nguyên tố hóa trị I
| Số Proton | Tên nguyên tố | Ký hiệu hóa học | Nguyên tử khối | Hóa trị | Số hóa trị |
|---|---|---|---|---|
| 1 | Hidro | H | 1 | I | 1 |
| 3 | Liti | Li | 7 | I | 1 |
| 9 | Flo | F | 19 | I | 1 |
| 11 | Natri | Na | 23 | I | 1 |
| 17 | Clo | Cl | 35,5 | I | 1 |
| 19 | Kali | K | 39 | I | 1 |
| 35 | Brom | Br | 80 | I | 1 |
| 47 | Bạc | Ag | 108 | I | 1 |
Nhóm nguyên tử hóa trị I
Thông thường chúng ta sẽ gặp những nhóm nguyên tử như: -OH, -HSO4, -Cl . . . và bảng hóa trị dưới đây sẽ là tổng hợp những nhóm nguyên tử có hóa trị I mà chúng ta thường gặp.
| STT | Tên nhóm | Công thức hóa học | Khối lượng Mol | Hóa trị | Số hóa trị |
|---|---|---|---|---|
| 1 | Hidroxit | -OH | M=16(O)+1(H) = 17 | I | 1 |
| 2 | Nitrit | -NO2 | M=14(N)+32(2-O) = 46 | I | 1 |
| 3 | Nitrat | -NO3 | M=14(N)+48(3-O) = 62 | I | 1 |
| 4 | Đi-Hidro-Phốtphát (Dihidrophotphat) | -H2PO4 | M=2(2-H)+31(P)+64(4-O) = 97 | I | 1 |
| 5 | Đi-Hidro-Photphorơ | -H2PO3 | M=2(2-H)+31(P)+48(3-O) = 81 | I | 1 |
| 6 | Hidro Sunfat | -HSO4 | M=1(H)+32(S)+64(4-O) = 97 | I | 1 |
| 7 | Hidro Sunfit | -HSO3 | M=1(H)+32(S)+48(3-O) = 81 | I | 1 |
| 8 | Hidro Cacbonat | -HCO3 | M=1(H)+12(C)+48(3-O) = 61 | I | 1 |
Học thuộc bảng hóa trị trên sẽ giúp chúng ta hình dung nhanh chóng và giải những bài tập rất dễ dàng. Các em hãy cố gắng, tranh thủ học càng sớm càng tốt nhé. Thật ra thì trước sau gì cũng phải học nên mình đầu tư chút thời gian ngay từ đầu để học bảng hóa trị sẽ giúp các em có nhiều thời gian để tìm hiểu về các dạng bài tạp hóa học sau này hơn!
Cách học thuộc hóa trị đơn giản nhất
Hiện nay, trên mạng xã hội có rất nhiều bài ca hóa trị được thầy cô sáng tác với mục đích tốt giúp học sinh đam mê hơn với môn hóa học. Tuy nhiên, với mỗi thầy cô sẽ có phong cách khác nhau nên những bài ca hóa trị cũng khác nhau.
Trong đời học sinh, tôi đã từng rất thành công với bài ca hóa trị sau đây. Các em tham khảo để học tốt môn hóa nhé.
Kali, Iot, Hiđro
Natri với Bạc, Clo một loài
Có hóa trị I bạn ơi
Nhớ ghi cho rõ kẻo rồi phân vân
Magie, Chì, Kẽm, Thủy ngân
Canxi, Đồng ấy cũng gần Bari
Cuối cùng thêm chú Oxi
Hóa trị II ấy có gì khó khăn
Bác Nhôm hóa trị III lần
Ghi sâu trí nhớ khi cần có ngay
Cacbon, Silic này đây
Là hóa trị IV không ngày nào quên
Sắt kia kể cũng quen tên
II, III lên xuống thật phiền lắm thay
Nitơ rắc rối nhất đời
I, II, III, IV khi thì là V
Lưu huỳnh lắm lúc chơi khăm
Lúc II, lúc VI khi nằm thứ IV
Photpho nói tới không dư
Nếu ai hỏi đến thì ừ rằng V
Bạn ơi cố gắng học chăm
Bài ca hóa trị suốt năm rất cần
Xem chi tiết tại Bài ca hóa trị
Sau khi các em học thuộc lòng bài ca hóa trị trên thì hóa trị của những nguyên tố có trong bảng hóa trị bên trên các em sẽ thuộc lòng. Mình không cần phải dùng bảng để tra cứu hay “” bài nữa nhé!

Với đam mê truyền đạt và chia sẻ những kiến thức hóa học hữu ích với mọi người, TC Chemistry không chỉ giới hạn việc chia sẻ kiến thức hóa học từ cơ bản đến nâng cao, mà còn cung cấp câu hỏi, đề thi thử và phương trình phản ứng hóa học để giúp người đọc hiểu sâu về chủ đề và phát triển kỹ năng trong lĩnh vực này.