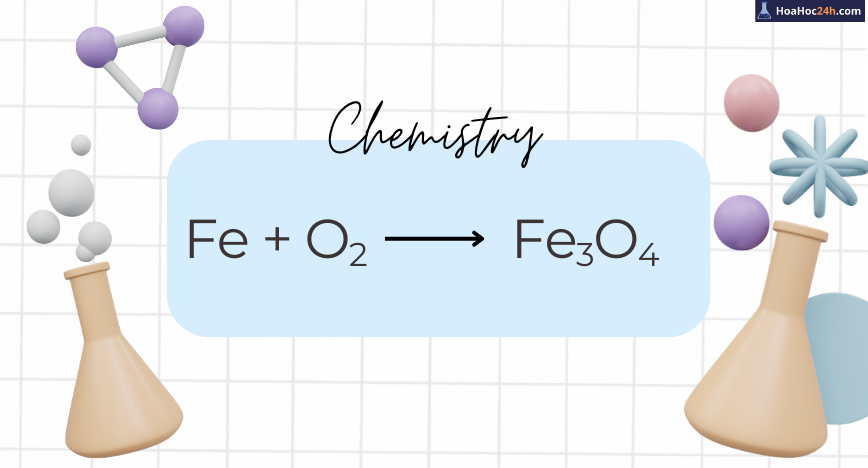Phản ứng giữa Oxit bazơ như FeO với Axit mạnh như HCl là phản ứng trung hòa đặc trưng trong Hóa học vô cơ, xảy ra dễ dàng ở điều kiện thường. Đây là một ví dụ cơ bản trong nhóm phản ứng giữa oxit bazơ + axit → muối + nước, thường gặp trong […]
Phương trình hóa học: Từ điển tìm kiếm PTHH chi tiết nhất
Phản ứng hóa học là quá trình biến đổi chất này thành chất khác cùng với những bài học trước đó như Công thức hóa học, Hóa trị ... là những bài học sẽ giúp các em hoàn thiện bài Phương Trình Hóa Học đơn giản hơn rất nhiều.
Định nghĩa phương trình hóa học
Phương trình hóa học hay còn được gọi là phương trình biểu diễn phản ứng hóa học là một phương trình gồm có 2 vế phân biệt bởi dấu mũi tên đánh theo chiều từ trái sang phải. Ở vế trái là chất tham gia phản ứng còn vế bên phải là chất tạo thành gọi là sản phẩm sau phản ứng.
Để đồng nhất các kí hiệu, người ta quy ước sử dụng công thức hóa học của các chất để biểu diễn một phản ứng hóa học qua phương trình. Bên cạnh đó, chúng ta sử dụng những hệ số đặt trước công thức hóa học đó để đảm bảo số nguyên tử tham gia phải bằng số nguyên tử sau phản ứng.
Phương trình hóa học đầu tiên được viết bời Jean Beguin vào năm 1615 trong ấn bản sách giáo khoa của ông. Phương trình hóa học được thể hiện còn thô sơ, các bạn hãy xem hình ảnh bên dưới về phương trình hóa học đầu tiên nhé.
Cách lập phương trình hóa học
Kiến thức cần có
- Công thức hóa học
- Hiểu về phương trình phản ứng
Trước tiên, chúng ta thường thấy rằng mọi phương trình hóa học đều được thiết lập qua lời nói, thể hiện trên giấy bút bằng chữ nên ta sẽ có được phương trình chữ của phản ứng hóa học.
Sau đó, dựa vào công thức hóa học của các chất được gọi tên chúng ta sẽ được sơ đồ của phản ứng. Sau đó, chúng ta thiết lập cân bằng nguyên tử của mỗi nguyên tố trước và sau khi phản ứng kết thúc. Như vậy, chúng ta đã lập được phương trình hóa học rồi nhé.
Các bước lập phương trình hóa học
Để lập được phương trình hóa học, các bạn cần tiến hành 3 bước và 3 bước này sẽ được cụ thể hóa qua ví dụ sau đây.
Sắt tác dụng với oxi dư ở nhiệt độ cao tạo ra hợp chất sắt (III) oxit có công thức hóa học là Fe2O3
Bước 1: Lập phương trình chữ và viết sơ đồ của phản ứng
- Phương trình chữ của phản ứng hóa học sắt và oxi
Sắt + Oxi → Sắt (III) Oxit [Fe2O3]
- Sơ đồ của phản ứng thể hiện bằng công thức hóa học
Fe + O2 → Fe2O3
Lưu ý: Khi các em làm quen việc lập phương trình, thì chúng ta không cần viết phương trình chữ nữa. Chúng ta viết luôn sơ đồ của phản ứng hóa học thể hiện qua công thức cho nhanh.
Bước 2: Cân bằng phản ứng là cân bằng số nguyên tử của mỗi nguyên tố.
Ta thấy, số nguyên tử của sắt và oxi ở cả 2 vế đều không bằng nhau do vậy ta phải thêm các hệ số vào trước công thức hóa học để cho số nguyên tử 2 bên cân bằng.
Tay nhận thấy rằng, số nguyên tử oxi lớn hơn số nguyên tử sắt nên ta sẽ cân bằng từ nguyên tố này trước nhé. Ta có số nguyên tử oxi ở phía bên trái là 2 còn số nguyên tử oxi ở phía bên phải là 3. Chúng ta tìm bội chung nhỏ nhất của 2 và 3 ở đây là 6.
Lấy bội chung nhỏ nhất chia cho số nguyên tử oxi ở mỗi bên đó chính là số hiệu cần đặt trước công thức hóa học của oxi hoặc hợp chất chứa oxi để cân bằng nguyên tử oxi ở mỗi bên.
Sau bước này ta sẽ được phương trình như sau: Fe + 3O2 → 2Fe2O3
Tiếp đó, ta thấy số nguyên tử của nguyên tố sắt bên phải là 4. Bên trái là 1 do vậy thêm số 4 vào công thức hóa học của Sắt là số nguyên tử ở hai vế phương trình đã cân bằng.
Sau khi cần bằng hoàn chỉnh phương trình trên ta được phương trình hóa học như sau:
4Fe + 3O2 → 2Fe2O3
Bước 3: Viết phương trình hóa học
4Fe + 3O2 → 2Fe2O3
Lưu ý quan trọng:
- Ở phương trình hóa học, công thức hóa học còn thể hiện trạng thái của các chất do vậy chúng ta không viết 6O vì oxi ở dạng phân tử khí O2
- Viết hệ số cân bằng cao bằng công thức hóa học của đơn chất hoặc hợp chất.
- Nếu trong hợp chất có các nhóm nguyên tử như -(OH), =(SO4), -(NO3) ... thì chúng ta còi đây là một đơn vị để cân bằng.
Ý nghĩa của phương trình hóa học
Phương trình hóa học cho chúng ta biết được tỷ lệ về số nguyên tử, số phân tử giữa các chất trong một phản ứng hóa học. tỷ lệ này cũng chính là tỷ lệ hệ số mỗi chất trong phương trình.
Ở ví dụ trên, 4Fe + 3O2 → 2Fe2O3 ta có thể nói như sau:
Bốn nguyên tử sắt tác dụng với 3 phân tử khí oxi sẽ tạo thành 2 phân tử
Sắt (III) oxit. Tỷ lệ: 4:3:2
Từ điển phương trình hóa học
Dưới đây là những phương trình hóa học thường gặp nhất được cân bằng chỉ số và có điều kiện xảy ra phản ứng. Đây sẽ là kho tư liệu cần thiết cho các bạn học sinh mỗi khi thắc mắc về phương trình nào đó.
Fe2O3 + CO → FeO + CO2↑
Phản ứng giữa Sắt(III) Oxit (Fe₂O₃) và Cacbon Monoxit (CO) là một phản ứng oxi hóa – khử. Trong điều kiện nhiệt độ cao và môi trường kiểm soát, CO khử Fe₂O₃ để tạo ra Sắt(II) Oxit (FeO) và khí Cacbon Dioxit (CO₂↑).Trong đó Fe³⁺ chuyển thành Fe²⁺, và C²⁺ trong CO bị oxi hóa […]
Fe + O2 → Fe3O4
Phản ứng giữa Sắt (Fe) và khí Oxi (O₂) không chỉ là phản ứng oxi hóa – khử điển hình mà còn thuộc nhóm phản ứng được chú trọng trong giảng dạy với nhiều dạng bài tập vận dụng phong phú. Trong điều kiện thích hợp, sắt phản ứng với oxi để tạo thành oxit […]
FeCO3 → FeO + CO2
Phản ứng nhiệt phân sắt(II) cacbonat là một phản ứng quan trọng trong chuỗi phản ứng luyện kim và có ý nghĩa sâu rộng trong công nghiệp. Phản ứng thể hiện bản chất của quá trình phân hủy muối cacbonat dưới nhiệt, đồng thời là cơ sở để nghiên cứu các phản ứng khử sâu […]
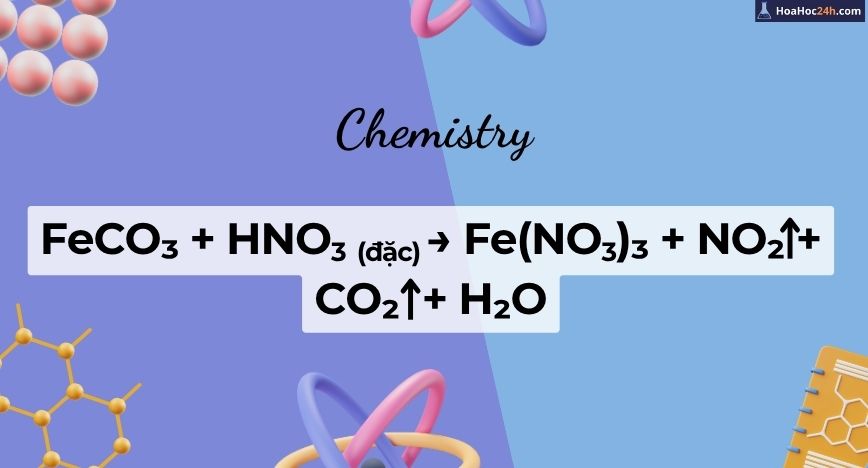
FeCO3 + HNO3 → Fe(NO3)3 + NO2 + CO2 + H2O
Phản ứng giữa sắt(II) cacbonat và axit nitric dẫn đến sự hình thành muối sắt(III) Nitrat, đồng thời giải phóng khí sunfurơ dioxit (NO₂), cacbon dioxit (CO₂) và nước. Mặc dù thoạt nhìn đây có vẻ là phản ứng axit – bazơ, thực chất lại là một chuỗi phản ứng oxi hóa – khử dị […]