Phản ứng Al + HCl là phản ứng hóa học từ Al ra AlCl3 được thực hiện bằng cách cho kim loại Al tác dụng với dung dịch HCl ở điều kiện bình thường rất dễ thực hiện ở trong phòng thí nghiệm. Đọc tiếp bài viết để khám phá thêm về phản ứng hóa học này nhé!
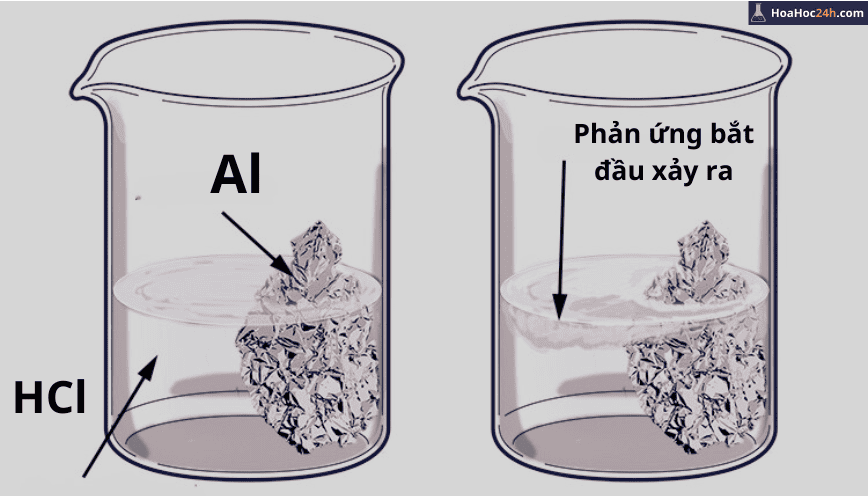
Phương trình hóa học Al + HCl
2Al + 6HCl → 2AlCl3 + 3H2
Phân loại phản ứng
Phản ứng Al + HCl được xếp vào nhóm phản ứng thế hoặc phản ứng oxi hóa – khử.
Al + HCl là một phản ứng thế?
Ở đây, chúng ta thấy ngay được nguyên tử Al đã thay thế nguyên từ H trong phân tử Axit hay nói cách khác là kim loại đẩy hidro ra khỏi gốc axit. Thay thế vào hidro trong gốc axit là một nguyên tử Al liên kết được với 3 phân tử Clorua tạo thành công thức là AlCl3.
Al + HCl là một phản ứng oxi hóa khử?
Đúng vậy, Al + HCl là một phản ứng oxi hóa khử bởi khi phản ứng xả ra chúng ta có được quá trình trao đổi electron giữa các chất mà cụ thể ở đây là:
Al – 3e → Al+3
H+ +2e → H2
Trong quá trình trao đổi electron trên ta thấy nhôm đã nhường đi 3 electron và H+ đã nhận về 2 electron để tạo thành 1 phân tử khí hidro H2. Như vậy, chất oxi hóa và chất khử đã rõ ràng do đó Al + HCl là một phản ứng oxi hóa khử nha.
Điều kiện phản ứng Al + HCl là gì?
Phản ứng Al + HCl xảy ra ở điều kiện bình thường, không cần thêm chất xúc tác hay thêm bất kỳ điều kiện nào khác nữa. Lưu ý một điều rằng, phản ứng xảy ra nhanh hơn nhiều lần nếu chúng ta cung cấp thêm nhiệt độ.
Cách thực hiện phản ứng Al + HCl như nào?
Để thực hiện được phản ứng Al + HCl chúng ta cần chuẩn bị:
– 1 ống nghiệm sạch và những hóa chất cần thiết: Al ở dạng bột hoặc thanh – Dung dịch axit HCl.
Thực hiện thí nghiệm Al + HCl bằng cách cho một thanh nhôm vào trong dung dịch HCl sẽ quan sát được hiện tượng thanh nhôm tan dần và có bọt khí thoát ra là H2. Trong dung dịch thu được sau khi phản ứng xảy ra hoàn toàn chắc chắn thu được muối AlCl3 nha.
Bài tập vận dụng
Ví dụ 1: Phát biểu nào sau đây là đúng?
A. Nhôm và crom đều phản ứng với dung dịch HCl theo cùng tỉ lệ số mol.
B. Hỗn hợp gồm Ba(NO3)2 và NaHCO3 có thể tan hoàn toàn trong nước dư.
C. Chỉ dùng dung dịch NaOH để phân biệt được hỗn hợp gồm Mg, Al2O3 và MgO.
D. Cr(III) oxit tan được trong dung dịch NaOH loãng ở nhiệt độ thường.
Hướng dẫn giải
Chọn B.
A sai, 2Al + 6HCl → 2AlCl3 + 3H2; 2Cr + 2HCl → CrCl2 + H2.
C sai, Al2O3 tan trong NaOH còn Mg, MgO thì không tan trong NaOH → Không phân biệt được.
D sai, Cr(III) oxit tan được trong dung dịch NaOH đặc, nóng.
Ví dụ 2: Cho các phản ứng sau:
(1). 4HCl + PbO2 → PbCl2 + Cl2 + 2H2O
(2). HCl + NH4HCO3 → NH4Cl + CO2 + H2O
(3). 2HCl + 2HNO3 → 2NO2 + Cl2 + 2H2O
(4). 2HCl + Zn → ZnCl2 + H2
(5). 4HCl + MnO2 → MnCl2 + Cl2 + 2H2O.
(6). 2HCl + Fe → FeCl2 + H2.
(7). 14HCl + K2Cr2O7 → 2KCl + 2CrCl3 + 3Cl2 + 7H2O.
(8). 6HCl + 2Al → 2AlCl3 + 3H2.
(9). 16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O.
Số phản ứng trong đó HCl thể hiện tính oxi hóa, và số phản ứng HCl thể hiện tính khử là bao nhiêu?
Hướng dẫn giải
5 phản ứng HCl thể hiện tính khử, 3 phản ứng HCl thể hiện tính oxi hóa.
HCl thể hiện tính khử khi có khí Cl2 bay ra bao gồm các phản ứng:
(3). 2HCl + 2HNO3 → 2NO2 + Cl2 + 2H2O
(9). 16HCl + 2KMnO4 → 2KCl + 2MnCl2 + 5Cl2 + 8H2O.
(5). 4HCl + MnO2 → MnCl2 + Cl2 + 2H2O.
(7). 14HCl + K2Cr2O7 → 2KCl + 2CrCl3 + 3Cl2 + 7H2O.
(1). 4HCl + PbO2 → PbCl2 + Cl2 + 2H2O
HCl thể hiện tính oxi hóa khi có khí H2 bay ra bao gồm:
(4). 2HCl + Zn → ZnCl2 + H2
(8). 6HCl + 2Al → 2AlCl3 + 3H2.
(6). 2HCl + Fe → FeCl2 + H2.
Ví dụ 3: Cho 5,4 gam Al hòa tan trong dung dịch axit HCl dư thu được V lít khí H2. Hỏi giá trị V bằng bao nhiêu?
A. 1,12 lit.
B. 2,24 lit.
C. 3,36 lit.
D. 6,72 lit.
Hướng dẫn giải
Chọn D.

Với đam mê truyền đạt và chia sẻ những kiến thức hóa học hữu ích với mọi người, TC Chemistry không chỉ giới hạn việc chia sẻ kiến thức hóa học từ cơ bản đến nâng cao, mà còn cung cấp câu hỏi, đề thi thử và phương trình phản ứng hóa học để giúp người đọc hiểu sâu về chủ đề và phát triển kỹ năng trong lĩnh vực này.